كاربرد PCR در بيوتكنولوژی
زيست فناوري (بيوتكنولوژي) از جمله واژههاي پر سرو صداي سال هاي اخير است. اين واژه را درست يا نادرست به مفهوم همه چيز براي مردم به كار ميبرند. زيستفناوري را در يك تعريف كلي به كارگيري اندامگان يا ارگانيسم يا فرايندهاي زيستي در صنايع توليدي يا خدماتي دانستهاند. تعريف ساده اين پديده نوين عبارت است از: دانشي كه كاربرد يكپارچه زيست شيمي ، ميكروب شناسي و فناوري هاي توليد را در سيستم هاي زيستي به دليل استفادهاي كه در سرشت بين رشتهاي علوم دارند ، مطالعه ميكنند. در تعريف ديگر ، زيست فناوري را چنين تشريح كردهاند:
فنوني كه از موجودات زنده براي ساخت يا تغيير محصولات، ارتقا كيفي گياهان يا حيوانات و تغيير صفات ميكروارگانيسم ها براي كاربردهاي ويژه استفاده ميكند.
زيست فناوري داراي دو جزء است: يك جزء آن در پي دستيابي به بهترين كاتاليزور براي يك فرايند يا عملكرد ويژه است و جزء ديگر، سيستم يا واكنشگري است كه كاتاليزورها در آن عمل ميكنند.

واژه بيوتكنولوژي (زيست فناوري) نخستين بار در سال 1919 توسط Karl Ereky به مفهوم كاربرد علوم زيستي و اثر متقابل آن ها در فناوري هاي ساخت بشر به كار برده شد.
به طور كلي زيست فناوري يكي از محورهاي اساسي توسعه در بسياري از كشورها قلمداد شده و در تنظيم راهكارها و برنامه هاي ملي ، توجه جدي به آن معطوف شده است.
بيوتكنولوژي ، دانشي برگرفته از گرايش هاي مختلف در شاخه هاي علوم زيستي است كه در ارتباط با به كارگيري ارگانيزم هاي زنده ، اندامك هاي آن ها ، مولكول ها و فـرايـنـدهـاي زيـسـتـي جـهـت بـهـبـود و تـوسعه خدمات پزشكي ، داروسازي ، صنعتي ، شيميايي و كشاورزي است.
بيوتكنولوژی پزشكی
كـاربـرد بـيـوتـكـنـولـوژي در پـزشـكـي بـه وسـعـت عـلـم پزشكي بوده و حتي اين علم با سرعت روزافزون بر وسعت و دامنه علم پزشكي ميافزايد.
از مهمترين كاربردهاي بيوتكنولوژي در پزشكي ميتوان به موارد زير اشاره كرد:
تـأثـيـر دگـرگـون كـنـنـده در امـر پيشگيري از بيماري هاي ميكروبي ، بيماري هاي ژنتيكي ، بيماري هاي تغذيه اي و متابوليسمي و بيماري هاي روحي رواني و ...
تـأثـيـر دگرگون كننده در امر درمان بيماري هاي عفوني ، ژنتيكي ، سوء تغذيه و متابوليسم و نازائي
تأثير دگرگون كننده در پزشكي قانوني
تأثير دگرگون كننده در پزشكي زيبائي
عناوين مطرح در بيوتكنولوژي پزشكي كه هركدام نياز به توصيف كامل دارند به طور عـمـده عـبارتند از: ژن درماني ، واكسن هاي نوتركيب ، بيو انفورماتيك ، ژنوميكس ، پـروتـئـومـيـكـس ، بـيومدسين و بيوفارماسوتيكال. امروزه پيشرفتهاي پزشكي به مدد بـيـوتـكـنـولـوژي در حـال سـرعـت گـرفـتـن اسـت. پـزشـكـي سـنـتـي به تدريج جاي خود را به پزشكي مولكولي خواهد داد. درآينده نه چندان دور مكانيسم هيچ نوعي از بيماري ها نـاشـنـاخـتـه نـخـواهـد مـانـد. پـزشـكـي سنتي به طور عمده به دنبال علائم و نشانه هاي بيماريها بوده و از روي آن به استنتاج وجود بيماري و عامل بيماريزا ميپرداخت و در مواردي به دليل ناشناخته بودن عوامل بيماري ها ، مكـانيسـمهـا و سيستمهاي كنترلي آن ها ، مبارزه تنها بر عليه علائم و نشانهها صورت ميگرفت.
امروزه به كمك بيوتكنولوژي ، علم پزشكي درحـال شناخت ريشهاي ترين بخش از حيات و مـظـــاهـــر آن اســـت. بـــا كـشـــف كـــامــل تــوالــي ژنـوم انسـان در سـال 2001 ، هـم اكنـون دانشمندان بـيـوتـكـنولـوژيـسـت بـــه دنـبـــال شـنـــاســـائـــي ژن هـــاي مسئول صفت هاي مختلف و نيز ژن هاي مسئول نـواقـص گـونـاگـون انـسـانـي هـسـتند. تا به حال ژن هاي مسئول ايجاد بيماريهاي بسياري شامل سـرطـان هـا ، بـيـماريهاي قلبي عروقي ، تنفسي ، رواني و ... شناسائي شدهاند.
بــا شـنــاســائــي تــكتــك ايــن ژن هــا و سـپـس شـنــاســائــي پـروتئيـن هـاي حـاصلـه از ايـن ژن هـا داروهـاي كـامـلا انـتـخـابـي و مـؤثـر براي مقابله با يــك بـيـمــاري ســاخـتــه مــيشــونــد. ايـن مـبـارزه در سطح پروتئين و فنوتيپاست ، راه ديگر مبارزه استفاده از ژن درماني است.
بيمـاري هـاي ژنتيكـي بسياري درحال حاضر بـه عنـوان كانديد براي ژن درماني درنظر گرفته شـــدهانــد. تـقــريـبــا هــركــدام از مــا تـعــدادي ژن نــاقــص در بــدن خــود داريــم كــه بـرخـي از آن هـا خـصــوصـيــات خــود را در فـنــوتـيــب مــا آشـكـار نكردهاند و برخي ديگر كم يا زياد ، خصوصيات خود را در فنوتيپ آشكار كرده اند. تقريبا از هر 10 نفر ، يك نفر داراي اختلالات ژنتيكي تظاهر يــافـتــه اســت و تـقــريـبــا 5% مـراجعـه كـودكـان بـه بـيـمــارسـتــان هــا بــه خــاطــر نـقــص در يــك تـك ژن است.
اطلاعات اوليه
اگر در يك مدل سازي تعداد زيادي مولكول و متغير داشته باشيم ، ممكن است جهت به دست آوردن مدل بهينه مجبور به انجام آزمايش هاي اضافي گرديم كه اهميت بسيار كمي در نتايج ما داشته باشد. اما چگونه و به چه روشي مي توان بهترين و موثرترين آن ها را مشخص كرد. ابزار مناسب استفاده از PCR و استفاده از PCA است. در اين روش مي توان به جاي داخل كردن مثلا 100 پارامتر ، با انتقال مناسب محور دكارتي ، آن ها را به 4 پارامتر كاهش داد بدون آنكه اين كاهش در نتيجه و صحت كار و مدل ارائه شده اختلالي ايجاد كند.
تعداد زيادي دستگاه Real Time PCR موجود است كه در شكل 1 ، يك نمونه از آن نشان داده شده است.
PCR در امــور جـنــايــي ، پـزشكـي مـولكـولـي ، بـيــوسـيـسـتـمــاتـيــك گـيـاهـي و جـانـوري و حـتـي مـيتـوان در ايجـاد جهـش هـاي ژني و برطرف كردن و انتقال ژن هاي مخرب و جايگزيني آن ها با ژن سالم از آن ها استفاده كرد.
دستگاه PCR شامل يك سيستم چرخه دمايي (Thermo Cycler) است كه نمونه ژنوم را به منظور بـاز شـدن رشتـه هـاي DNA بـه دمـاي 95 درجـه ميرساند ، بعد دما به 45 درجه مي رسد تا آنزيم پــلــيــمــــراز زنــجــيــــره هـــاي از هـــم بـــاز شـــده را همانندسازي كند و بعد در دماي 70 درجه انيل مي شود. اين چرخه دمايي موجب تكثير متناوب توالي خاصي از DNA مي شود كه پرايمر خاص آن در محلول وجود دارد.
در اين روش نمونه اي از DNA را كه داراي توالي مورد نظر است به مخلوط واكنش اضافه مي كنيم. با تكرار چرخه همانند سازي چهار نسخه توليد مي شود و به همين ترتيب فرايند به صورت نمايي (Exponential) تعداد نسخه ها را در هر بار همانند سازي دو برابر مي كند و بعد از 30 ساعت بيش از يك ميليون نسخه از هر مولكول توليد مي شود.
تاريخچه
در گذشته معمولا از روش هاي شيميايي براي توليد قطعات نوكلئوتيدي استفاده ميكردند اما اين روش ها پر زحمت بوده و نياز به مدت زمان طولاني داشتند. از سال 1980 به بعد به طور عمده از روش PCR در آزمايشگاههاي زيست شناسي مولكولي استفاده ميشود. PCR در دهه 80 ميلادي توسط كري موليس اختراع شد.
كشف PCR انقلابي در علوم تشخيص كلينيكي بيماري ها ، پزشكي ، علوم جنايي و پليسي ، ميكروبيولوژي و بسياري صنايع ديگر ايجاد كرد كه به خاطر آن جايزه نوبل به مبتكر آن اهدا شد. هم اكنون بيشتر ماركرهاي مولكولي بر پايه PCR هستند. ماركرهايي از قبيل SSR , SNP, AFLP و ... بر پايه PCR هستند.
الـبـتــه الان ديـگــر ايــن روش مــاننـد گـذشتـه نيسـت و يـك روش پيـش پـا افتـاده در آزمايشگاههاي مولكولي است. امروزه روش هاي آن ارتقاء يافته و مدل هاي زيادي از آن انجام مي شود و طرز كار آن با پايه همانند سازي تك رشته DNA است. معمولا اول زنـجـيره را باز مي كنند و توالي هاي خاصي را به عنوان پرايمر طراحي مي كنند كه اختصاصي آن ژن يا توالي است كه مي خواهيم بررسي كنيم و بعدا آن را تكثير كرده و توسط الكتروفورز در مقابل يك كنترل مي سنجند. يكي از روش هاي خوب اين مدل Real Time PCR است كه حتي مي توان به صورت كمي و دقيق ، هدف مورد نظر را اندازه گرفت.
PCR يكي از سه تكنيك تشخيص مستقيم پاتوژن هاي ميكروبي در نمونه هاي باليني اســت. دو روش ديـگــر عـبــارتـنــد از: اپـيـدمـيـولـوژي مـولـكـولـي و بـررسـي اكـتـشـافـي اسيدنوكلئيك.
مزاياي روش PCR عبارتند از: بررسي يك روزه ، ارزان بودن نسبي ، آساني انجام و اختصاصي بودن فوق العاده اين روش.
PCR مخفف Polymerase Chain Reaction يا واكنش هاي زنجيره اي پليمراز است و به طور ساده تكثير قطعات DNA با گرم و سرد كردن، متناوب است. PCR ، تكنيكي است كه به واسطه آن مي توان از يك رشته DNA يا از يك رشته RNA ، تعداد زيادي رشته DNA به دست آورد ، به شرطي كه دو انتهاي رشته DNA كه قصد تكثيرش را داريم كاملا شناخته شده باشد. با اين روش مي توان يك ژن را به اندازه اي تكثير كرد تا بتوان با استفاده از روشهايي مانند الكتروفورز مشاهده كرد. شما يك تار مو را از فاصله 6 متري نمي توانيد ببينيد اما يك دسته ميلياردي از مو كنار هم به خوبي مشاهده مي شوند. اصل PCR هم بر اين مبنا استوار است. براي تكثير يك قطعه خاص ، ابتدا يك پرايمر از DNA موردنظر ، طراحي مي شود و با استفاده از PCR تكثير مي شود.
مراحل PCR
مرحله دناتوراسيون DNA: در مرحله اول براي مدت كوتاهي (30 ثانيه) قطعات DNA را در درجه حرارت 94 درجه سانتيگراد حرارت ميدهند تا دو زنجيره DNA از هم باز نشود.
مرحله پرايمر و مرحله اتصال دو قطعه نوكلئوتيدی: اين قطعات معمولا از 25 - 18 باز آلي تشكيل ميشوند و ميتوانند به قطعات مكمل خود كه بر روي ژن مورد نظر قرار ميگيرند ، اتصال يابند. قطعهاي كه در آن PCR به تعداد زياد ساخته ميشود ، مرحله اتصال پرايمرها كوتاه بوده و در حدود 30 ثانيه در دماي 65 - 30 درجه سانتيگراد صورت ميگيرد.
مرحله پليمريزاسيون يا مرحله سنتز: در اين مـرحلـه ، با دخالت آنزيم DNA پليمراز بر روي رشـتــه DNA الـگــو و سـنـتــز DNA بــا اسـتـفـاده از نـوكـلـئـوتـيـد تـري فـسـفـاتهـايي كه در محلول وجود دارند ، صورت ميگيرد و براي سنتز DNA هـميشه يك رشته DNA به صورت الگو و يك قطعه پلي نوكلئوتيدي به عنوان پرايمر مورد نياز است.
ادامه PCR بعد از چرخه اول
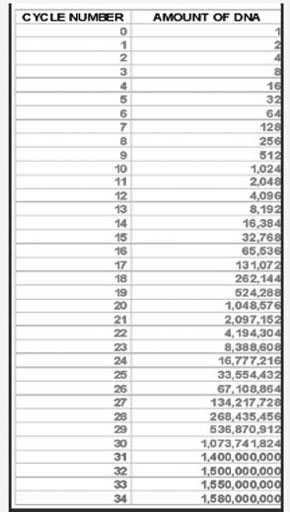
بعد از اين 3 مرحله ، چرخه اول تمام ميشود و چـرخـه هاي بعدي تكرار چرخه اول است. بدين صورت به دنبال چرخههاي متعدد PCR قطعه DNA مورد نظر به طور تصاعدي افزايش مييابد. يعني از 20 چرخه ، ژن مورد نظر داراي بـــيــــــش از یک مــيــلـيـــون خـواهــد بــود كـه در جـدول زیر ، افـزايـش تعـداد DNA نشان داده شده است. بنابراين روش PCR روشي كارا در ازدياد يك قطعه از DNA است.
كاربردهای مهم PCR
تهيـه نسخههای متعدد از يک ژن مورد نظـر: گاهي براي مطالعات بيولوژي مولكولي لازم است كه يك ژن با نسخههاي نسبتا زياد در دسترس باشد. بدين منظور ميتوان با استفاده از روش PCR ، ژن مورد نظر را در مقايسه با بقيه ژنها تكثير كرد.
بررسی حضور يا عدم حضور يک ژن: با استفاده از اين روش ميتوان تشخيص داد كه آيا يك ژن در يك سلول حضور دارد يا نه؟ گاهي نيز از اين مطالعات براي بررسي وجود ژنهاي مختلف باكتريها يا ويروسها در بدن افراد استفاده ميكنند.
تشخيص بيماریهای قبل از تولد: با استفاده از PCR و به كار گرفتن پرايمرهاي مربوط به يك ژن بيمار و پرايمرهاي مربوط به ژن سالم آن ، ميتوان از تولد كودكان داراي بيماريهاي ژنتيكي جلوگيري كرد. براي اين كار بعد از لقاح تخمك در آزمايشگاه و بعد از رسيدن تخمك به حالت 10 سلولي ، يك سلول را جدا كرده و با استفاده از پرايمرها از ژن مورد نظر PCR صورت ميگيرد. اگر بعد از PCR منحصرا ژن سالم تكثير پيدا كرد، اين مفهوم هموزيگوت بودن سلولهاي جنيني و سالم بودن آنها است.
تشخيـص عامل يک بيماری ناشناخته: فرض كنيد بيمار شما به يك بيماري ناشناخته گرفتار است و شما احتمال مي دهيد كه عامل بيماري ويروس است. اين ويروس را نمي شود در آزمايشگاه كشت داد ، بنابراين با روش PCR مي توان احتمال اين ويروس را در عرض یک ساعت كنترل كرد. يعني نمونه اي از بدن بيمار و همچنين قطعهاي از ژن اين ويروس را كه پرايمر نام دارد به دستگاه مي دهيم. اگر حتي فقط یک عدد از اين ويروس در نمونه بيمار باشد ، دستگاه از ژن آن ميليارد ها كپي تهيه مي كند. سپس مي توان اين حجم زياد ژن را در صفحه فيلم فلورسنت حاصل از الكتروفروز مشاهده كرد. اگر باند هاي DNA روي ژن ديده شد مطمئن مي شويد كه بيمار ناقل اين ويروس است.
تعيين جنسيت جنين: به طور معمول چند تخمك با چند اسپرم در آزمايشگاه لقاح مييابند و سپس اجازه تكثير به سلول تخم داده و با رسيدن تخم به مرحله ده سلولي ، يكي از سلولها را جدا كرده و به وسيله پرايمرهاي ويژه مربوط به كروموزوم Y مورد PCR قرار ميگيرد. كروموزوم Y منحصرا در سلولهاي نر ديده ميشود. اگر قطعه توليد نشده در PCR به وسيله الكتروفورز و به طور دقيقتر توسط ساترن بلوتينگ تشخيص داده شد، جنين از نوع پسر و در غير اين صورت داراي كروموزومهاي XX خواهد بود.
تشخيص بيماری ها
كشت ميكروب ها كه جهت تشخيص بيماريهاي عفوني در بيشتر آزمايشگاه ها به كار ميرود زمان بر بوده و همچنين باعث افزايش تعداد ميكروب هاي بيماري زا و غير بيماريزا در شرايط آزمايشگاهي مي شود. امروزه در برخي آزمايشگاه ها روش PCR جايگزين روشهاي كشت شده است. يعني قطعه اي از ژن مربوط به ميكروب بيماري زا مورد شناسايي قرار گرفته و پرايمرهاي مربوط توليد مي شوند. با استفاده از اين پرايمرها مي توان تشخيص داد كه آيا مثلا ويروس ايدز در داخل بدن وجود دارد يا نه؟
از ديگر موارد استفاده از PCR مي توان ، مطالعه نسبت خويشاوندي در تفحص شهدا ، تشخيص بيماري هاي ژنتيكي در اثر ازدواج هاي فاميلي ، تعيين هويت ، تعيين سن و قد ، جـرم شنـاسـي از طـريـق آثار باقيمانده از قاتل ، تكثير ژن براي ايجاد آنزيم ، تشخيص سرطانها و ايجاد جهش هاي هدف دار را نام برد.
مواد لازم PCR
1- بافر PCR: شرايط يوني ph مناسب را براي واكنش PCR فراهم مي كند. بافر به صورت x10 ساخته مي شود. اين بافر داراي گليسيرول براي سنگيني كار و داراي رنگ براي مشهود سازي DNA است.
2- دزوكسی نوكلئوتيد تری فسفات: كه به صورت مخلوطي از چهار باز در بازار وجوددارد تا كنار هم چيده شوند و رشته مكمل را ايجاد كنند .
3- آغازگرها Primer: پرايمرها قطعات سنتز شده اي از بازهاي آلي اند كه بر اساس قطعه مورد نظر الگوهاي هدف ساخته مي شوند كه معمولا با طول 3015 نوكلئوتيد هستند كه به DNA الگو متصل مي شوند. طول پرايمرها بسيار مهم است و هر چه طول پرايمر بلند باشد اختصاصي تر عمل مي كند.
پرايمرها دو عمل انجام مي دهند. اول اين كه محل ژني را كه بايد تكثير شود مشخص ميكنند و دوم اين كه اندازه قطعات تكثير شونده را تعيين مي كنند. بايد توجه داشت دو پرايمر داراي نقطه ذوب نزديك به هم باشند. پرايمر مورد نظر توسط كامپيوتر انتخاب مي شود.
4- Tag DNA Polymerase: يك آنزيم مقاوم به دما است كه همانند سازي DNA را انجام ميدهد. آنزيم Tag پليمراز باعث مي شود به راحتي واكنش PCR به طور اتوماتيك انجام شود .
5- Mgcl2 كلريد منيزيم نقش كوفاكتوري در فعاليت آنزيم Tag دارد. اثر متقابل رشته DNA الـگــو و آغـازگـر را افـزايـش مـي دهـد. غلظـت كلـريـدمنيـزيـم اثـر زيـادي بـرروي اختصاصي شدن و در نهايت بازده واكنش PCR دارد. غلظت زياد آن اثر بازدارندگي برروي فعاليت آنزيم تگ DNA پلي مراز دارد و مقدار محصول نهايي را كاهش مي دهد.
6- دی ان آ الگو Template DNA: بسته به هدف آزمايش از منابع مورد نياز با استفاده از يكي از روش هاي مرسوم استخراج مي شود. معمولا به ازاي هر واكنش 5% واحد يا 1% ميكرو ليتر استفاده مي شود.
7- لوله های واكنش: لوله هاي كوچك 5% ميلي ليتر
8- سمپلر و سر سمپلرهاي يكبار مصرف مخصوص آن ها كه براي برداشتن مقادير بسيار كم استفاده مي شود.
9- دستگاه چرخش حرارتي
10- ميكرو فيوژ
11- روغن معدنی Mineral Oil: يك قطره روي مخلوط واكنش اضافه مي شود تا از تبخير نمونه در دستگاه چرخش حرارتي Thermal Cycler جلوگيري مي شود. معمولا 50 تا 60 ميكروليتر به محلول واكنش 100 ميكروليتري اضافه مي شود .
مشكل PCR و راه حل آن
اشكال PCR ، آلودگي نمونههاي مورد بررسي توسط قطعات DNA خارجي است. اگر قبلا در داخل دستگاهي PCR يك نمونه انجام گرفته باشد و ذره كوچكي از آن در داخل دستگاه باقي بماند در PCR نمونه بعدي مشكل ايجاد خواهد كرد. براي رفع مشكل ، امروزه از ظروف يك بار مصرف استفاده ميشود. كليه ظروف قبل از استفاده اتوكلاو ميشوند تا سلولها و مولكول هاي موجود در آن ها ، تا حد ممكن غير فعال ميشوند.
يـكــي از روشهــاي پـيـشـنهـادي انجـام PCR داخـلــي يـا Nested PCR اسـت. از ايـن روش بـا استفـاده از دو پرايمر قطعهاي از DNA را تكثير مــيدهـنــد و سـپــس قـطـعــهاي ديـگــر در داخـل DNAهــاي تـكـثـيــر شــده PCR مــيشــود. بــديــن صورت احتمال آلودگي كاهش مييابد.
منبع: ماهنامه مهندسی پزشکی
کلمات کلیدی: biomedical engineering ، مهندسی پزشکی ، آشنایی با مهندسی پزشکی ، معرفی مهندسی پزشکی ، مهندسی پزشکی گرایش بالینی ، مهندسی پزشکی گرایش بیومکانیک ، مهندسی پزشکی گرایش بیوالکتریک ، مهندسی پزشکی گرایش بیومتریال (بیومواد) ، مهندسی پزشکی ایران ، مهندسی پزشکی دانشگاه پیام نور ، پایگاه آموزشی و اطلاع رسانی مهندسی پزشکی ، اخبار و تازه های مهندسی پزشکی ، مقالات مهندسی پزشکی ، آموزش مهندسی پزشکی ، دانلود کتاب های مهندسی پزشکی ، دانلود جزوه های مهندسی پزشکی ، دانلود نمونه سوالات امتحانی مهندسی پزشکی ، پی سی آر ، PCR ، بیوتکنولوژی ، کاربرد PCR در تکنولوژی ، زیست فناوری ، ژنتیک ، ژن ، DNA ، دی ان ای ، RNA ، بیماری های ژنتیکی


.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)